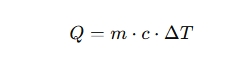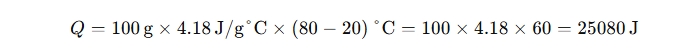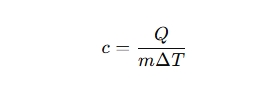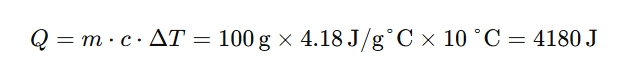第一节 分子热运动
一、物质的构成
物质的构成可以从微观和宏观两个层次进行理解。物质是由不同的基本组成单元构成的,下面是简要概述:
1. 宏观层次:物质的三态
在宏观层次,物质通常存在于三种常见的状态:
- 固态:物质的分子、原子或离子紧密排列,通常具有固定的形状和体积。例如冰、金属。
- 液态:物质的分子之间存在一定的间距,分子可以自由流动,体积固定,但形状随容器变化。例如水、油。
- 气态:物质的分子相距较远,且自由运动,既不固定形状也不固定体积。例如空气、氮气。
此外,还有等离子态,这是一种由带电粒子(电子和离子)组成的物质状态,例如在高温条件下产生的电弧、太阳等。
2. 微观层次:物质的基本构成
从微观角度看,物质是由基本粒子构成的,这些粒子之间通过相互作用形成不同的结构。主要组成成分包括:
a. 原子
- 原子是物质的基本单位,由原子核和围绕原子核旋转的电子组成。原子核内由质子和中子构成,电子则携带负电荷,围绕原子核旋转。
- 原子的种类通过质子数(即原子序数)来区分,不同的原子具有不同的化学性质。
b. 分子
- 分子是由两个或多个原子通过化学键结合而成的单位。分子是化学反应中的基本单元。
- 比如,水(H₂O)由两个氢原子和一个氧原子组成,空气中的氧气(O₂)由两个氧原子组成。
c. 离子
- 离子是带有电荷的原子或分子。离子可以是正离子(失去电子)或负离子(获得电子)。
- 比如,盐中的氯化钠(NaCl)是由钠离子(Na⁺)和氯离子(Cl⁻)组成。
d. 基本粒子
- 进一步深入,原子核内的质子和中子由更基本的粒子——夸克组成,而电子则是属于基本粒子之一,被归类为轻子。
- 基本粒子包括质子、中子、电子、夸克、光子等。
3. 物质的结构
- 物质的宏观性质(如状态、形状、密度等)是由微观粒子的排列和相互作用决定的。
- 在固体中,原子或分子通常呈规则排列(如晶体结构),而在液体和气体中,粒子之间的排列较为松散,分子或原子之间的相互作用力较弱。
总结
物质是由原子、分子、离子等微观粒子构成的。原子是物质的基本单元,它们通过化学键结合成分子。不同的物质是由不同类型和排列的微观粒子组成的,这些微观粒子之间的相互作用决定了物质的各种性质和状态。
二、分子热运动
分子热运动是指物质中的分子由于温度的影响而进行的无规则运动。这个运动是物质内部分子、原子或离子随机运动的结果,温度越高,分子的运动越剧烈。分子热运动包括以下几种基本形式:
1. 平动运动
分子在空间中沿直线自由移动,特别是在气体和液体中,分子作无规则的平动运动。
2. 振动运动
在固体中,分子或原子围绕其平衡位置作周期性的振动,形成固体物质的晶格振动。
3. 转动运动
分子可以绕其中心旋转,这种运动在气体和液体中都存在,尤其是在较大的分子中。
特点:
- 无规则性:分子运动方向和速度是随机的。
- 与温度相关:温度越高,分子平均动能越大,运动越剧烈。
- 宏观现象:分子热运动是热现象的基础,解释了温度、扩散、压强等现象。
总结:
分子热运动是物质的微观粒子由于热能的作用而进行的随机运动,体现了物质的热行为,直接与物质的温度、压强和体积等宏观性质相关。
三、分子间的作用力
什么是分子间作用力?
想象一下,一滴墨水滴入水中,瞬间散开。这背后的原因就是分子间存在着相互作用的力,我们称之为分子间作用力。
分子间作用力是指存在于分子与分子之间的一种吸引力或排斥力。虽然这种力很微小,但它对物质的性质有着非常重要的影响。
第二节 内能
一、内能
内能(Internal Energy)是指物质内部所有粒子(如原子、分子、离子等)所具有的总能量。它是物质在一定条件下(如温度、压力、体积等)所表现出来的能量,通常用符号 U 表示。
内能不仅包括物质的宏观能量,还涉及微观粒子(例如分子、原子、电子等)之间的各种形式的能量。
内能的组成
内能主要包括两大部分:
- 动能:物质内部粒子由于热运动(平动、振动、转动)所具有的动能。它与温度直接相关,温度越高,分子的运动越剧烈,动能越大。
- 分子平动能:分子做无规则的平移运动。
- 分子振动能:分子内部原子围绕平衡位置作振动运动(尤其在固体中显著)。
- 分子转动能:分子绕其中心旋转的能量。
- 势能:物质内部粒子之间相互作用的能量(例如分子之间的吸引或排斥力)。这部分能量与分子或原子之间的相互作用力密切相关。
- 在分子之间,势能通常与分子间的距离、化学键等因素有关。例如,氢键、范德华力等都属于分子间的势能。
内能与热力学的关系
在热力学中,内能是一个状态函数,意味着它只依赖于物质的当前状态(如温度、压力、体积等),与物质的历史过程无关。例如,气体的内能仅与气体的温度和体积有关,而与气体如何达到这一状态无关。
内能的变化
在热力学过程中,内能的变化通常与热量的交换和外界做功有关:
ΔU=Q−W
其中:
- ΔU:内能的变化
- Q:热量(系统吸收的热量为正,释放的为负)
- W:功(系统对外界做功为正,外界对系统做功为负)
内能的例子
- 在加热气体时,分子的热运动增强,导致气体的内能增加。
- 在物质发生相变(如冰融化成水)时,虽然温度不变,但内能会增加,因为分子间的势能发生变化。
总结
内能是物质的总能量,包括物质内部粒子的动能和势能。它与温度、压强、体积等状态变量相关,在热力学中,内能是描述能量交换和转化的重要概念。
二、物体内能的改变
物体的内能改变,通常是由于物体与外界交换热量或做功所引起的。内能的变化可以通过**热量(Q)和做功(W)**来描述,这些过程是热力学中的基本概念。
内能变化的基本关系
根据热力学第一定律,内能的变化 (ΔU) 与热量的交换 (Q) 和系统对外界做功 (W) 之间的关系是:ΔU=Q−W
-
Q:热量,物体与外界交换的热能。
- Q>0:系统吸热(内能增加)。
- Q<0:系统放热(内能减少)。
-
W:功,物体对外界做功或外界对物体做功。
- W>0:物体对外界做功(内能减少)。
- W<0:外界对物体做功(内能增加)。
内能改变的原因
物体的内能变化主要有两个原因:
-
热量的传递(热交换):
- 当物体吸收热量时,分子的热运动增强,内能增加。比如加热气体或加热固体,会增加分子运动的动能,从而增加内能。
- 当物体释放热量时,分子的热运动减弱,内能减少。比如物体冷却时,分子动能减少,内能也会随之减少。
-
功的转移:
- 当物体对外做功时(例如气体膨胀推动活塞),能量从物体转移到外界,内能减少。比如气体膨胀做功的过程中,气体分子对外界做功,导致内能减少。
- 当外界对物体做功时(例如压缩气体),能量从外界传递到物体,内能增加。比如气体被压缩时,外界做功使气体分子的运动增强,导致内能增加。
物体内能改变的具体情况
-
热量传递
- 加热过程:当物体吸热时(例如加热气体或水),物体内部分子的运动加剧,内能增加。加热时,温度升高,内能增加。
- 冷却过程:当物体放热时(例如冰融化成水时或气体冷却时),物体内部分子的运动减弱,内能减少。放热时,温度下降,内能减少。
-
做功过程
- 膨胀做功:当气体或液体膨胀并推动外部物体(例如活塞),气体对外做功,部分内能转化为机械功,导致气体的内能减少。
- 压缩做功:当外界对气体或液体做功(如压缩气体时),气体分子的运动增强,内能增加。
-
相变过程 在物质的相变过程中(如从固态到液态或从液态到气态),内能也会发生变化,即使温度不发生变化。这是因为相变过程中,物质的分子结构发生变化,势能改变。
- 熔化:固体吸收热量变为液体,内能增加。
- 蒸发:液体吸热变为气体,内能增加。
- 凝固:液体放热变为固体,内能减少。
- 凝结:气体放热变为液体,内能减少。
例子:气体膨胀和压缩
-
等温膨胀(温度不变):在等温过程中,气体分子的平均动能不变,但体积增大,气体对外做功,内能不变。这里的热量传递与做功的量相等。
-
绝热膨胀(没有热量交换):在绝热膨胀过程中,气体通过膨胀对外做功,内能减少,因为没有热量输入来补偿做功,温度也会下降。
-
绝热压缩(没有热量交换):在绝热压缩过程中,气体被压缩,分子间的碰撞增加,内能增加,温度也会升高。
总结
物体内能的变化主要是通过热量的交换和做功过程来实现的。内能增加通常伴随有热量的吸收或外界对物体做功,而内能减少则通常伴随有热量的释放或物体对外界做功。
第三节 比热容
一、比热容
比热容(Specific Heat Capacity)是指单位质量的物质在温度变化时吸收或释放的热量。简而言之,比热容描述了物质对温度变化的“抵抗”能力。比热容越大,物质在温度变化时所需吸收或释放的热量就越多。
比热容的定义
比热容 c 是单位质量的物质在温度变化 ΔT 时,吸收或释放的热量 Q 与其质量 m 和温度变化量之间的比值:
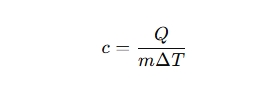
其中:
- c:比热容,单位是焦耳每千克每摄氏度(J/kg·°C),或焦耳每克每摄氏度(J/g·°C)。
- Q:热量,单位是焦耳(J)。
- m:物质的质量,单位是千克(kg)或克(g)。
- ΔT:温度变化,单位是摄氏度(°C)或开尔文(K)。
比热容的意义
比热容表示了物质储存热量的能力。比热容大的物质需要吸收或释放更多的热量才能使其温度变化一定的幅度。不同物质的比热容不同,通常水的比热容较大,这也是水在温度变化时能起到缓冲作用的原因之一。
比热容的性质
- 高比热容的物质:这些物质在吸收或释放相同量的热量时,温度变化较小。例如,水的比热容相对较高,约为 4.18 J/g·°C。
- 低比热容的物质:这些物质的温度变化较大。比如大多数金属(如铁、铜)的比热容较低。
水的比热容
水的比热容非常大,约为 4.18 J/g·°C,这意味着每克水的温度上升 1°C 需要吸收 4.18 焦耳的热量。这一特性使得水具有很好的热调节能力,能够缓慢加热或冷却,并在自然界中起到调节温度的作用。举例来说:
- 水是地球表面大气温度变化的“温控器”,它能缓慢吸收太阳能量,从而避免地球温度的剧烈波动。
比热容的应用
-
热量计算:通过比热容可以计算物体在温度变化过程中吸收或释放的热量。例如,假设有 100 克水加热 10°C,所吸收的热量是:
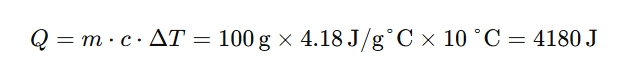
-
温度调节:比热容高的物质(如水)常用于热容量大、需要缓慢加热或冷却的设备中,例如热水瓶、温控系统等。
-
地球气候:水的高比热容帮助调节地球的气候,使得气温变化不会过于剧烈。海洋吸收太阳能后,缓慢释放热量,保持了地球的温暖。
比热容的测量
比热容可以通过实验测量,常见的实验方法是定压加热法或定容加热法。在实验中,测量在物质吸收或释放热量时,物体的质量、温度变化以及所吸收的热量,从而计算出比热容。
比热容与物质的状态
- 气体、液体和固体的比热容不同。一般情况下:
- 固体的比热容较小,因为固体分子运动的自由度较低。
- 液体的比热容较大,液体分子之间的相互作用较强,能量储存能力较强。
- 气体的比热容通常较大,尤其是在高温或低压下,气体的分子运动自由度较大。
总结
比热容是物质的一个重要物理特性,它衡量了单位质量的物质在温度变化时所需吸收或释放的热量。比热容大的物质在温度变化时储存的能量较多,而比热容小的物质在温度变化时会更迅速地改变温度。
二、热量的计算
热量(Heat, Q)是指在物体或系统之间进行热交换时,所传递的能量。热量的大小与物体的质量、比热容、温度变化等因素有关。常见的热量计算方法依据热量与物理量之间的关系,可以应用于多种场景,如加热、冷却、相变等。
1. 热量计算公式
加热或冷却过程(温度变化)
当物体的温度发生变化时,热量的计算公式为:
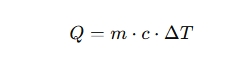
其中:
- Q:热量,单位为焦耳(J)。
- m:物体的质量,单位为千克(kg)或克(g)。
- c:比热容,单位为焦耳每千克每摄氏度(J/kg·°C)或焦耳每克每摄氏度(J/g·°C)。
- ΔT:温度变化,单位为摄氏度(°C)或开尔文(K)。
应用场景:
- 当你加热 100 克水,温度从 20°C 升高到 80°C,计算所需的热量。
假设水的比热容为 4.18 J/g·°C,则:
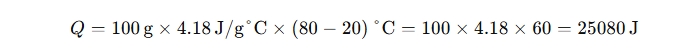
2. 总结
热量的计算主要依赖于热量传递的方式和物质的特性。在物质加热或冷却时,热量与物质的质量、比热容和温度变化有关;在相变过程中,热量与物质的质量和潜热相关。通过这些公式,我们可以计算物质在不同过程中所吸收或释放的热量,进而分析和解决热力学中的实际问题。
全章总结
1. 分子动理论的基本观点
- 常见的物质是由大量的分子、原子构成的。
- 构成物质的分子在不停地做热运动。
- 分子间存在着引力和斥力。
2. 内能
物体的内能是物理内部所有分子热运动的动能和分子势能的总和。改变物体的内能有两种方法:做功和热传递。
3. 比热容
一定质量的某种物质,在温度升高(或降低)时吸收(或放出)的热量与它的质量和升高(或降低)的温度乘积之比,叫做这种物质的比热容。温度变化时,热量的计算公式参考前面内容。